KW:健康食品・天天素清脂交嚢・Mysore・HCA・mazindol・マジンドール・シブトラミン・sibutramine・ヒドロキシクエン酸・hydrocitic acid・ガルシニア
Q:新聞等で健康被害報道がされている『天天素清脂こう嚢』について
A:『天天素清脂こう嚢』(コウは月偏に交)について、次の報告がされている。
中国製とみられるダイエット用健康食品「天天素」が原因と疑われる下痢や腹痛などの健康被害の報告が8都県で10人にのぼっていることが26日、厚生労働省のまとめで分かった。このうち東京都では10代の女性が死亡した。いずれも違法な向精神薬が含まれていたうえ、インターネット上で取引されていた。死亡した女性は、約2カ月半前から天天素を使用しており、13キロやせたという。都は天天素が死亡につながった恐れがあるとみている。
厚労省には、東京のほか、岡山(2人)、広島、富山、千葉、福島、群馬、愛知(2人)の各県から天天素を使用した女性の健康被害が報告されている。愛知県では10代の女性が入院中で、意識レベルが低下するなど重症という。
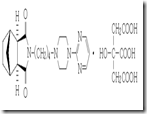
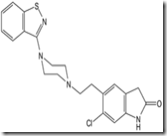
天天素はカプセル剤で、製造者として「野馬生物(広州)保健品有限公司」の表示がされている。これまでの検査で、国内では未承認の肥満症治療剤の「シブトラミン」と、法律で規制されている向精神薬「マジンドール」が検出されたため、厚労省は入手経路や販売業者を調べている[朝日新聞,2005.5.26.]。
『天天素』の表示成分について、直接現品確認をすることはできなかったが、HP上に公表された成分として、HCA及びインド南部が原産とされるMysoreから抽出されたフラボノイド・vitaminB1・vitaminB6・vitaminB12等各種ビタミン・鉄・亜鉛・カルシウム等とする紹介がされている。
*Mysore:インド南西部の都市、マイソール(Mysore)に由来する名称である。キツネノマゴ科ツンベルギア属の蔓性常緑多年草で、学名:Thunbergia mysorensis。和名:矢筈葛(ヤハズカズラ)。総状花序が1メートルほど伸び、元の方から順次開花する。黄色い花弁と暗赤褐色の苞が美しい花で、温暖な気候の地域では一年中見ることができるとされている。ただし、矢筈葛で検索すると学名:Thunbergia alata。英名:Black-eyed susan vine(黒い瞳のスーザン葛)、Clock vine等の結果が得られた。参照までに花の写真を引用する。

(Thunbergia mysorensis)

(Thunbergia alata:矢筈葛)
*HCA:ヒドロキシクエン酸(hydroxycitic acid)。本品は南アジア原産のオトギリソウ科の柑橘類ガルシニア・カンボジアの果実に含まれる有機酸で、“ガルシニア”とも呼ばれる。ヒドロキシクエン酸は、肝細胞・脂肪細胞の細胞質で行われるクエン酸からアセチルCoAを生成するATP-クエン酸リアーゼの反応を阻害することで知られている。クエン酸がアセチルCoAに変わる反応は、脂肪の材料である脂肪酸の合成に必須である。従って“ガルシニア”が血液中の脂肪を低下させたり、肥満を予防する可能性が考えられている。
“ガルシニア”によって、細胞質でのクエン酸のアセチルCoAへの転換が阻害されると、ミトコンドリアにクエン酸がたまることになる。クエン酸がミトコンドリアにたまると、ケトン体が体内に増加し、酸性体質になる可能性がある。しかし、“ガルシニア”によってケトン体が増加するという状況は実際にはあまり見られないとされている。“ガルシニア”はATP-クエン酸リアーゼを阻害する他に、膵臓リパーゼの反応を抑制して、食事中の脂肪の腸管吸収を抑制することが明らかにされている。
その他、“ガルシニア”は糖質が脂肪に変換されるのを防ぎ、エネルギーとして利用されやすくする働きがあるとされており、ウォーキングなどの有酸素運動との組み合わせにより体脂肪の燃焼効果が増大するとされている。脳下垂体を刺激し、空腹感を感じなくさせることが知られている。健康食品としてのガルシニアエキス摂取の目安量はヒドロキシクエン酸換算で、体重50kgの成人で1.5g/日を超えない量とする。ラットにおける実験で、ガルシニアの長期にわたる大量摂取で、ラット精巣に影響が見られたとする報告もされている。
*フラボノイド(flavonoid):この名称は高等植物に普通に現れるフラボンから由来しており、ベンゼン核2個が中間に炭素原子3個を挟んで直列に結合した色素化合物の総称名である。これに含まれるものはカルコン、フラバノン、フラバノノール、フラボン、フラボノール、イソフラボン、アントシアニジン類である。このうち色を持つものにはアントシアニジン(赤褐色-黒紫色)、フラボン(黄色-橙色)、フラボノール(黄色-橙色)及びカルコン(橙黄色-橙赤色)などがある。古くは黄色の色素化合物の総称名でアントキサンチンとも呼ばれていた。
その他、分析の結果、未表示の成分としてマジンドール(mazindol)・シブトラミン(sibutramine)・フェノールフタレイン(phenolphthalein)の存在が確認されたと報告されている。
*マジンドール(mazindol):食欲抑制剤。医療用医薬品。劇薬、第3種向精神薬(麻薬及び向精神薬取締法の向精神薬に該当。)、習慣性医薬品、指定医薬品、処方せん医薬品。
食欲中枢への直接作用及び神経終末におけるノルアドレナリン、ドパミン、セロトニンを介した機序により摂食抑制作用を示すとともに、消化吸収を抑制することにより摂取エネルギーを減少させ、肥満を是正すると考えられている。
重大な副作用:依存性、肺高血圧症。
その他の副作用:1.精神神経系(口渇感、頭痛、睡眠障害、脱力感、眠気、倦怠感、いらいら感、眩暈、ふらつき、神経過敏、激越、抑うつ、神経障害、振戦、幻覚、知覚異常、不安、痙攣)。2.消化器(便秘、悪心、嘔吐、胃部不快感、腹部膨満感、腹痛、下痢)。3.循環器(動悸、頻脈、胸痛、血圧上昇、脳卒中、狭心症、心筋梗塞、不整脈、心不全、心停止、顔面紅潮)。4.過敏症(発疹、掻痒感)。5.肝臓(AST・ALTの上昇)。6.泌尿器(排尿困難、頻尿)。7.その他(口中苦味感、発汗、性欲減退、咽頭不快感、寒気、脱毛、月経異常)。
*シブトラミン(sibutramine):肥満症治療剤。本薬は、わが国では承認されていない。
副作用:頭痛、口渇、便秘、不眠、鼻炎 等。そ の 他:米国の添付文書に警告として「血圧及び心拍数の増加」が記載されている。
*フェノールフタレイン(phenolphthalein):緩下剤。本品は水には不溶であるが、アルコールには可溶。小腸内で可溶性塩となり、平滑筋に対する直接の収縮作用と粘膜に対する刺激作用により腸運動を亢進させるので下剤として用いられた。米国において動物実験により発ガン性が報告され、国内においても製造が中止された。
表示された成分を見て、肥満解消可能と判断した根拠は、ヒドロキシクエン酸が配合されているということであろうが、未公表配合成分を見ると製造業者は、表標記の成分だけで効果が得られるということについて、全く信じていなかったということのようである。
『いわゆる健康食品』摂取で、肥満解消は無理だということをそろそろ理解すべきである。
1)http://www.asahi.com/life/update/0526/006.html?t5,2005.6.3.
2)http://drugmania.exblog.jp/,2005.6.6.
3)http://www.botanic.jp/plants-ma/thumys.htm,2005.6.6.
4)奥田拓道・監修:健康・栄養食品事典-機能性食品・特定保健用食品;東洋医学舎,2004-2005
5)澤 賀津子・他:サプリメント・ブック;日本文芸社,2003
6)薬科学大辞典 第2版;広川書店,1990
7)高久史麿・他監修:治療薬マニュアル;医学書院,2005
8)飯野靖彦・監訳:スカット・モンキーハンドブック;メディカル・サイエンス・インターナショナル,2003
9)http://wwhttp://www.r-dietetics.com/hca.htmw.r-dietetics.com/hca.htm,2005.6.6.
10)http://www3.pref.okinawa.jp/site/view/contview.jsp?cateid=93&id=8900&page=1,2005.6.6.
[015.9.HCA:2005.6.11.古泉秀夫]
参照資料として厚生労働省の発信文書を以下に添付する。
平成17年5月27日
厚生労働省医薬食品局監視指導・麻薬対策課
ダイエット用食品「天天素(天天素清脂こう嚢)」(マジンドール等を含有する無承認無許可医薬品)によると疑われる健康被害について
ダイエット用食品として販売されていた「天天素(天天素清脂こう嚢:てんてんそせいしこうのう)」については、5月24日に「マジンドール」「シブトラミン」等の医薬品成分が検出され、広島県等、全国各地から健康被害の事例が公表されております。また、5月26日には東京都からこの製品との因果関係が疑われる死亡事例が公表されております。
この製品による健康被害の拡大を防止するために、国民の皆様にこの製品を服用しないことなどの注意を呼びかけるQ&Aを作成しましたので、ご留意ください。
Q1.「天天素」とはどんな製品ですか。「天天素」の安全性は確認されているのでしょうか。
A.この製品はダイエット用食品としてインターネット等を通じて販売されていましたが、国立医薬品食品衛生研究所等で分析した結果、向精神薬の「マジンドール」と、わが国で承認されていない「シブトラミン」等の医薬品成分が検出されました。
医薬品は薬事法により、わが国で安全性、有効性等が審査されて承認された製品だけが流通可能ですが、この製品については無承認無許可医薬品であり、安全性等は全く確認されていません。
また、この製品を服用したことによると疑われる健康被害が報告されていますので、絶対に服用しないでください。
Q2.どのような健康被害が報告されているのでしょうか。
A.この製品を服用した方について、眩暈(めまい)、嘔吐(おうと)、下痢、腹痛、頭痛、不眠、動悸、口の渇き等の健康被害が報告されています。
また、この製品との因果関係が疑われる死亡事例、入院治療を受けられた事例も報告されています。
Q3. 「天天素」を服用したことがあるのですが、どうしたらいいでしょうか。
A.この製品の安全性は確認されておらず、健康被害を起こすおそれがありますので、絶対に服用しないでください。これまでに服用したと思われる方で、身体に異常を感じられている方は、医療機関を受診されるか、最寄りの保健所に相談ください。
Q4.「マジンドール」とはどんな医薬品成分ですか。副作用はどのようなことが知られていますか。
A.食欲抑制剤(麻薬及び向精神薬取締法の向精神薬に該当。)
適 応:食事療法、運動療法の効果が不十分な高度肥満症
副 作 用:口渇感、便秘、悪心・嘔吐、睡眠障害、胃部不快感 等
重大な副作用:依存性、肺高血圧症
用 法・用 量:成人1日1回0.5mg、1日最高1.5mgまで
Q5.「シブトラミン」とはどんな医薬品成分ですか。副作用はどのようなことが知られていますか。
A.肥満症治療剤(わが国では承認されていない成分)
米国の適応:肥満症の治療(肥満における体重減少及び体重減少の維持)
副 作 用:頭痛、口渇、便秘、不眠、鼻炎 等
米国の添付文書に警告として「血圧及び心拍数の増加」が記載されている。
Q6.この製品を他人に販売したり、譲渡したりすると法律違反になるのでしょうか。
A.この製品は薬事法上、無承認無許可の医薬品であると同時に、麻薬及び向精神薬取締法の向精神薬に該当します。従って、この製品を販売または譲渡したり、広告すること、輸入することは、薬事法、麻薬及び向精神薬取締法で禁じられています。